VITA 1600 Boulevard di Wilson, Seguito 500 Arlington, Virginia i 22209 Stati Uniti TEL: 703/276-1800. Facsimile: 703/243-1865 Internet di: pr-info@vita.org Understanding le Batterie
ISBN: 0-86619-225-5 [C]1985, Volontarii in Assistenza Tecnica
PREFACE
Questa carta è una di una serie pubblicata da Volontarii in Tecnico Assistenza per provvedere un'introduzione a specifico all'avanguardia le tecnologie di interesse a persone in paesi in sviluppo. Si intende che le carte siano usate come orientamenti per aiutare, persone scelgono tecnologie che sono appropriate alle loro situazioni. Non si intende che loro provvedano costruzione o la realizzazione, Persone di details. sono esortate per contattare VITA o un'organizzazione simile per informazioni ulteriore ed assistenza tecnica se loro scoperta che una tecnologia particolare sembra soddisfare le loro necessità. Le carte nella serie furono scritte, furono fatte una rassegna, e furono illustrate quasi completamente da VITA Volunteer esperti tecnici su un puramente basis. volontario che Alcuni 500 volontarii stati comportati nella produzione dei primi 100 titoli pubblicati, mentre offrendo approssimativamente 5,000 ore del loro time. il personale di VITA incluse Maria Giannuzzi come redattore, Suzanne Brooks che si occupa di typesetting e configurazione, Margaret Crouch come direttore di progetto. L'autore di questa carta, VITA Horace McCracken Spontaneo, è il presidente del McCracken Società Solare in Alturas, la California. Il coautore, VITA Joel Gordes Spontaneo, è attualmente il solare disegni analista per lo Stato dell'Ipoteca Solare di Connecticut Sussidio Program. I recensori sono anche VITA volunteers. Daniele Dunham ha fatto consultando in fonti solari ed alternative di energia per VITA ed AID. Lui ha vissuto e ha lavorato in India, Pakistan e Morocco. il Sig. Dunham ha preparato anche un all'avanguardia osservi su stills solare per Aiuto. Jacques Le Normand è Assistente Direttore al Fermi Istituto di Ricerca, Quebec, Canada quale indaga in energia rinnovabile. Lui ha soprinteso a lavoro con raccoglitori solari e ha scritto molto publiations su solare ed energia di vento, e la conservazione. Darrell G. Phippen è un ingegnere meccanico e specialista di sviluppo con che lavorano Cibo per l'Affamato in Scottsdale, Arizona. VITA è un'organizzazione privata, disinteressato che sostiene persone lavorando su problemi tecnici in paesi in sviluppo. le offerte di VITA informazioni ed assistenza puntarono ad individui utili e gruppi per selezionare e perfezionare le tecnologie appropriano loro situations. VITA mantiene un Servizio di Indagine internazionale, un centro di documentazione specializzato, ed un elenco computerizzato di volontario consulenti tecnici; maneggia progetti di campo a lungo termine; e pubblica una varietà di manuali tecnici e carte.
I. INTRODUZIONE DI
Batterie sono in uso dal molti anni, ma c'è oggi un richiesta più grande per il potere di batteria che mai prima. che Questo ha rinnovato interesse non solo è stato provocato da sviluppi nuovi ma anche dalla diversità di usi per batterie in borghese, industriale, e domande militari. Questa carta provvede una comprensione di base di batterie e tracce il loro sviluppo dai primi 1800s alla Ricerca di day. presente e sviluppo continua in un sforzo di risolvere l'inerente la debolezza di batterie, vale a dire come comprimere più energia in un pacco più piccolo. Una cella elettrica o batteria è un'apparecchiatura che trasforma il energia chimica contenne direttamente all'interno dei suoi materiali attivi in energia elettrica da vuole dire di una reazione di electrochemical. Questo tipo di reazione comporta il trasferimento di elettroni da uno materiale ad un'altra attraverso una soluzione che conduce. Historically, batterie ebbero un ruolo importante di giorni primi di elettrico sviluppo ambo negli Stati Uniti ed in Europa. Nel 1800 un scienziato italiano chiamato Volta scoprì quello da due bigliettai dissimili che immergono in una soluzione chimica un electromotive costringono (EMF) o tensione fu stabilita fra il due conductors. Figure 1 illustra una cella di Voltaic semplice. I bigliettai solidi della cella sono chiamati elettrodi ed il liquido che conduce l'elettrolito. che Una cella consiste di due elettrodi ed un electrolyte. Una batteria consiste di uno o più cells. La tensione della cella dipende sul materiale del elettrodi e l'elettrolito. La produzione corrente ed elettrica e il potere della cella è dipendente sulle dimensioni di piatto e il peso del materiale di elettrodo. Ci sono due tipi generali di batterie in uso oggi: il primario dattilografi o " cella " asciutta ed il deposito secondario battery. Un batteria primaria produce un corrente da azione di scarico quando uno degli elettrodi della cella è decomposto durante uso. Questo tipo di cella usare di nuovo ricaricando non può essere ripristinato ed il cella intera si deve scartare quando non è più active. Secondary celle, d'altra parte è chimicamente invertibile e può sia addebitato e licenziò su prima molti cicli di operazione essendo sostituito. Nella cella di tensione semplice mostrata in Figura 2, quando due dissimile
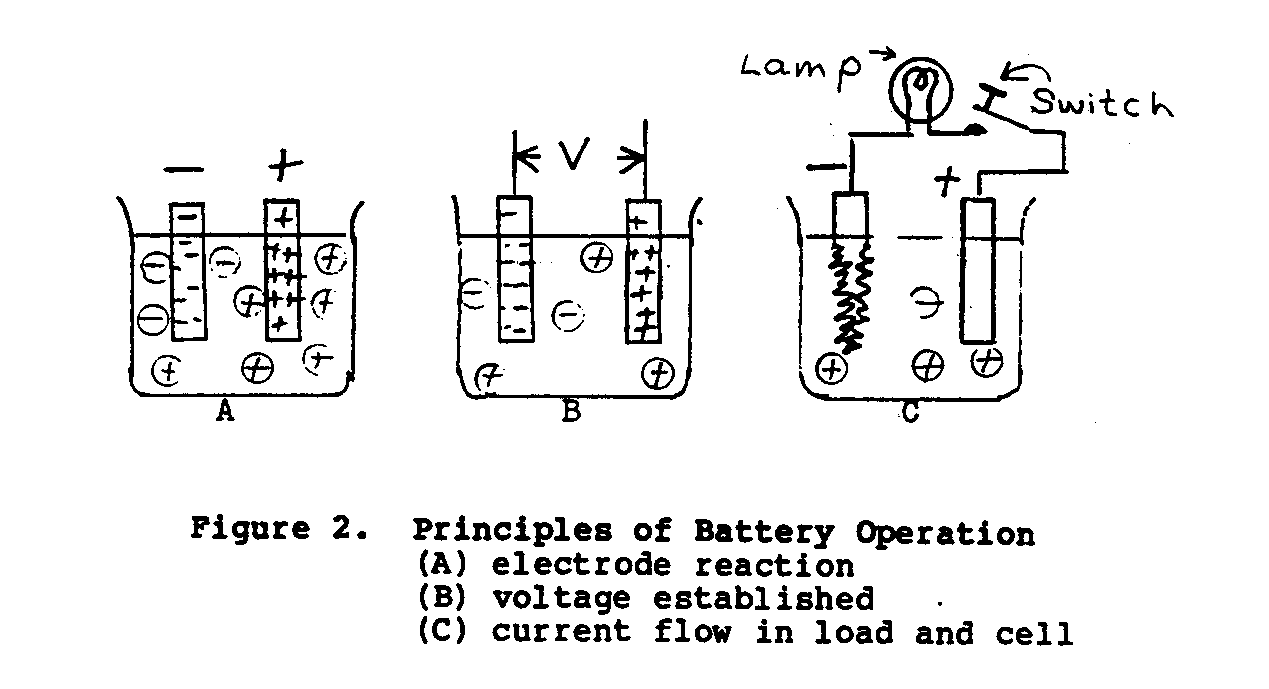
metalli, zinco e rame sono sospesi in un elettrolito di diluisca acido solforico, un potenziale di approxiamtely 1.10 volt esista tra gli elettrodi. L'elettrodo di zinco sarà negativo e l'elettrodo di rame sarà positivo. Quando il cambi nel circuito di carico esterno è chiuso, una volontà corrente fluisca attraverso il carico (apparecchiatura energia-assorbente) e batteria in concordanza alla Legge di Ohm. * Come il carico corrente continua a fluire, idrogeno come bolle apparirà e coprirà il piatto di rame, e il piatto di zinco gradualmente dissolverà. Lo svantaggio principale con questa cella è che la benzina forma bolle aumento l'interno resistenza della cella, causando produzione corrente per decrescere.
* La corrente continua fluente in un circuito elettrico è direttamente proporzionale alla tensione applicata al circuito. La costante della proporzionalità R, chiamò la resistenza elettrica, è dato dal V di equazione = RI dove V " è la tensione applicata e Io " sono il corrente.
II. VARIAZIONI DI TECNOLOGIA
BATTERIE PRIMARIE
Molti tipi diversi di primario-tipo che celle bagnate sono state sviluppate ed usato negli Stati Uniti. Most notable fra questi era il cella di gravità, la cella di ossido di caustico-rame, gli aria-depolarizzarono cella, e la cella di Lelanche. Ogni cella aveva operando suo proprio caratteristiche, e capacità correnti variarono da meno che uno ampere (l'ampere) per la cella di Lelanche a molti cento ampere per la cella di ossido di caustico-rame. che L'ufficio postale britannico ha sviluppato una cella bagnata noto come la cella del Daniele che offrì molto caratteristiche di funzionamento notevoli.
C'erano due difficoltà principali con la cella di primario-tipo costruzione, deterioramento da azione locale e polarizzazione di cella. Azione locale è un'azione chimica ed interna inerente a batterie; la vita della cella gradualmente è diminuita anche sebbene nessun carico è connesso ai suoi terminali. che azione Locale è definito come lo scarico di materiale attivo di entrambi piatto dovuto a dell'impurezza nell'elettrolito o materiale di piatto. Questo azione provoca la formazione di celle cortocircuitate che causano il metallo per deteriorare.
Polarizzazione di cella è causata da bolle di idrogeno che sono depositate sul catodo quando flussi correnti attraverso la cella. che Questo abbassa la tensione finale ed aumenti la resistenza interna del battery. metodi Vari per neutralizzare questo effetto che polarizza fu usato, o da costruzione chimica o meccanica che condotto allo sviluppo della cella aria-depolarizzata. Nella cella aria-depolarizzata, l'elettrodo fu fatto di un estremamente forma assorbente di carbone e fu sospeso sopra dell'elettrolito level. da quando l'elettrodo di carbone non stato immerso nell'elettrolito soluzione, polarizzazione della cella fu prevenuta. In operazione, ossigeno che circonda la superficie porosa del carbone elettrodo combina con l'idrogeno evoluto alla superficie di l'elettrodo di carbone ed elettrolito. che ventilazione Buona è stata richiesta mantenere un'aria soddisfacente approvvigiona per operazione.
Il Cella di carbone di Edison e la batteria di Carbonaire erano rappresentative del tipo aria-depolarizzato. Wet primario-dattilografano celle hanno grandemente stato sostituito dalla batteria di deposito di secondario-tipo. Il giorno " moderno cella asciutta " che fu sviluppata da Georges Lelanche nel 1868, è una modifica del Lelanche vecchio cella bagnata. La differenza è quell'acqua solamente sufficiente è aggiunta il elettrolito per inumidire una rigatura assorbente. La cella asciutta e moderna è principalmente l'estesamente usato di tutte le batterie primarie oggi a causa del loro costo basso, spettacolo affidabile, e molto esteso availability. che batterie di cella Asciutte sono fatte in stime di 1.5, 36, 7.5, 9, 22.5, 45, 67, e 90 volt.
Il tipo più comune di costruzione per una cella asciutta è mostrato in Figuri 3.
La cella in Figura 3 usi una verga di carbone per l'anodo o positivo terminale ed un fuori contenitore di zinco (il caso) per il negativo terminal. Il caso di zinco ha una rigatura interna di carta assorbente materiale che è reso saturo con l'elettrolito. Lo spazio tra gli elettrodi è riempito con una mistura di coca cola schiacciata, diossido di manganese, e grafite. Il Manganese di è aggiunto come un depolarizer. L'elettrolito è salammonic e cloruro di zinco. Il cima del caso è sigillata con un sigillando composto e lo zinco contenitore è incluso in un contenitore di carta. La tensione di un nuovo cella asciutta è 1.4 a 1.6 volt. Batterie di cella asciutte cadono in tre classi generali: (1) la pila batterie di solito 1-1/4 pollice in diametro e 2-1/2 pollici alto con una capacità corrente di approssimativamente 3 ampere-ore; (2) taglia grande celle, assegnate più comunemente a come il Numero 6 cella asciutta verso 2-1/2 pollici in diametro e 6 pollici alto con un stima corrente di approssimativamente 30 ampere-ore; e (3) il " dovere " pesante e tensione alta dattilografa che sarebbe una cella o una combinazione di celle, usato in servizio industriale con capacità correnti di 50 ampere-ore o greater. L'ampere-ora capacità è la percentuale di licenzi una batteria può mantenere per un periodo determinato di tempo, di solito otto hours. Per esempio, una 30 ampere-ora tassò batteria normalmente provvedere approssimativamente 3-1/2 ampere per otto ore. Come ordinariamente celle asciutte ed usate provvedono meno comunque, che la loro stima. La vita di mensola è limitata da azione locale e per quella ragione alcuni fabbricanti bollano una data di servizio sul coprire esterno di ogni cell. azione Locale provoca il deterioramento eventuale del batteria, e dopo approssimativamente un o due deposito di anni, la batteria diviene useless. siccome l'elettrodo di zinco forma parte dell'esterno muro, la sua distruzione graduale indebolisce la struttura di cella, e come la benzina di idrogeno sviluppata costruisce su pressione interna, può rottura e sparge i suoi contenuti corrosivi. Per questa ragione, attrezzatura non dovrebbe essere immagazzinato mai con celle asciutte su periodi lunghi di time. celle Asciutte non richiedono manutenzione e quando loro più operi è scartato e sostituì. Un tipo più recente di asciugi cella sviluppata è il Ruben o Mercurio cella (Figura 4) . dal quale Questa cella è stata sviluppata durante guerra mondiale II
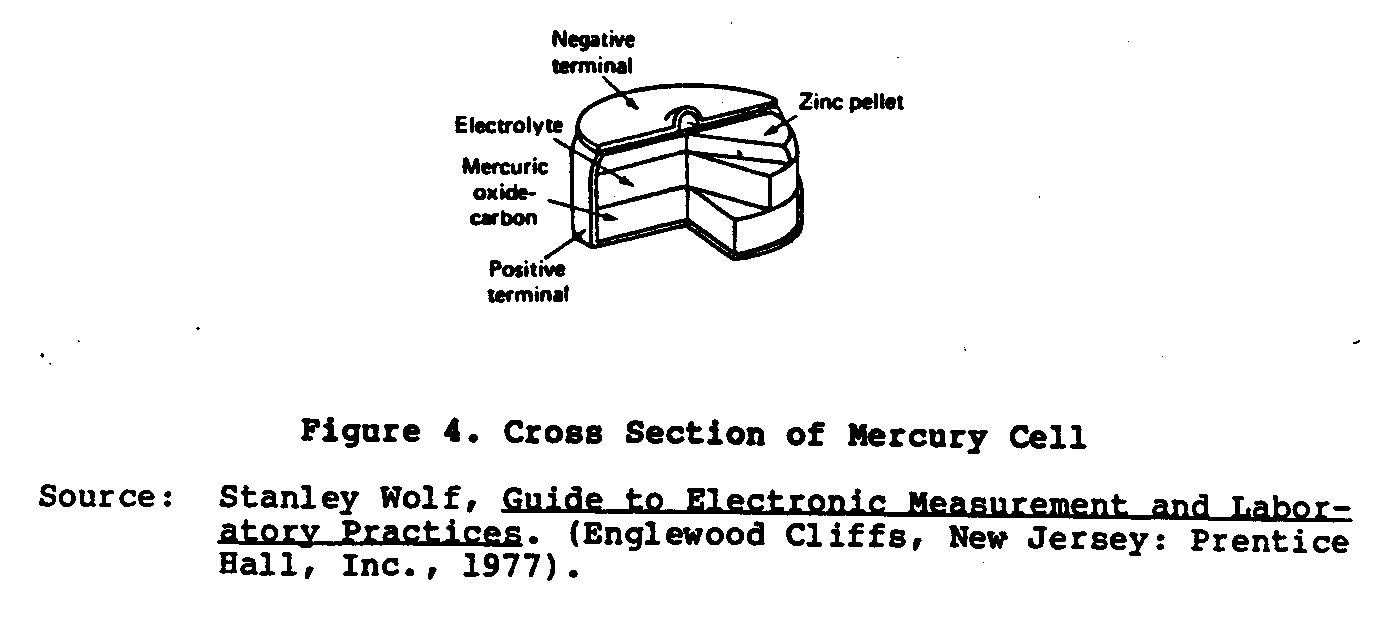
Laboratori di Ruben e P.R. Società di Mallory per operare piccolo attrezzatura elettronica che richiede il potere corrente ed alto. che Questa cella è fatto in due forme: il " anodo " di rotolo ed il " bottone dattilografano. " Il anodo è amalgamato zinco ed il catodo è un ossido mercurico materiale depolarizzato mescolò con grafite. L'elettrolito è un soluzione di idrossido di potassio (KOH) contenendo zincate di potassio. Queste celle sono lontano superiori al Lelanche cella dovendo asciutto alla loro taglia compatta, caratteristica di tensione piatta, e molto lungo mensola life. La tensione di nessuno-carico di queste celle è 1.34 volt. Molti sviluppi avanzati sono stati fatti in batterie piccole, ambo primario e secondario-dattilografa celle che includono il magnesio, alcalino l'argento-zinco, e lithium. Table 1 elenchi il caratteristiche e domande di queste celle.

BATTERIE DI DEPOSITO SECONDARIE
Fin da 1965, là è stato rinnovato interesse nell'usare deposito batterie nel potere systems. che Questo è perché il consumo di potere moderno comporta richieste di carico molto disuguali e carico di picco in aumento demands. Quando un sistema deve consegnare più potere (aumento in carico richiesta), il fornitore può soddisfare la richiesta da uno cambiando un generatore supplementare sopra il sistema o cambiando un addebitò banca di batteria sopra il line. Il secondo richiede un molto più piccolo investimento.
Il revival di batterie come unità di sistema di potere ha primariamente cominciato con sistemi indipendenti e piccoli come vento - o acqua-controllato generators. In tali sistemi, batterie di deposito compiono due functions. First importanti, durante periodi di richiesta di carico bassa la batteria di sistema può immagazzinare molta dell'energia generata, quali sarebbero persi altrimenti al sistema. Second, energia immagazzinato durante il periodo di via-picco è disponibile durante tempi di carico di picco demand. che L'importanza del secondo può essere illustrata con l'esempio quantitativo e seguente: Supponga il capacità della batteria ha una percentuale di potere di scarico uguale a metà della capacità di potere di generatore ([P.sub.B] = 0.5 [P.sub.G]) . Questo intende quello sotto le condizioni normali, durante periodi di richiesta di carico alta il combinazione di generatore-batteria può per molte ore serva un carico di su a 1.5 volte quello che potrebbe servire da solo il generatore.
Un'altra ragione per l'interesse aumentato in deposito secondario batterie sono il bisogno per il potere di riserva per alcuno del più nuovo technology. Per esempio, computer più moderni comportano della forma di " deposito volatile " di informazioni, quello è, le informazioni sono perse se il potere è removed. per proteggere contro questa possibilità, molti sistemi di computer usano " uninterruptible " motorizzano sistemi, basato su batterie di deposito, approvvigionare elettrico corrente al computer attrezzatura quando il potere commerciale è perso.
La batteria di deposito, costruita con celle bagnate e secondarie è simile in azione ad una cella primaria, ometta le azioni chimiche coinvolto è praticamente completamente invertibile. Once che la cella è licenziato, corrente da una fonte esterna, passò attraverso il cella nella direzione opposta, ripristinerà sostanzialmente il batteria alla sua condizione addebitata ed originale.
Ci sono attualmente tre tipi di batterie di deposito disponibile: (1) il tipo di piombo-acido; (2) il nichelio-ferro o batteria alcalina (Cella di Edison); e (3) il nichelio-cadmio o alcali-dattilografa (Nicad).
Batterie di piombo-acido
La batteria di piombo-acido è più estesamente gli usarono dattilografiamo di batteria oggi a causa del suo costo basso, l'affidabilità, spettacolo buon caratteristiche, e domanda larga. che Questa batteria è fabbricata in molte taglie e capacità che variano da 1 ampere-ora su a molte milli ampere-ore tassando. La cella di deposito usa reactive scroccano piombo per il negativo elettrodo (Pb), diossido di piombo per l'elettrodo positivo (Pb0), e diluisce acido solforico per l'elettrolito. L'elettrodo materiali hanno poco forza strutturale e devono essere sostenuti su piatti o grids. La griglia del piatto di batteria ha due funzioni: prima, sostiene il materiale di piatto attivo; e secondo, serve come un bigliettaio a connettere il terminale di piatto a tutti parti del materiale attivo.
Conduca piatti di batteria di deposito sono divisi in due tipi, il Plante (formò) ed il Faure (incollò), come mostrato in Figura 5. In
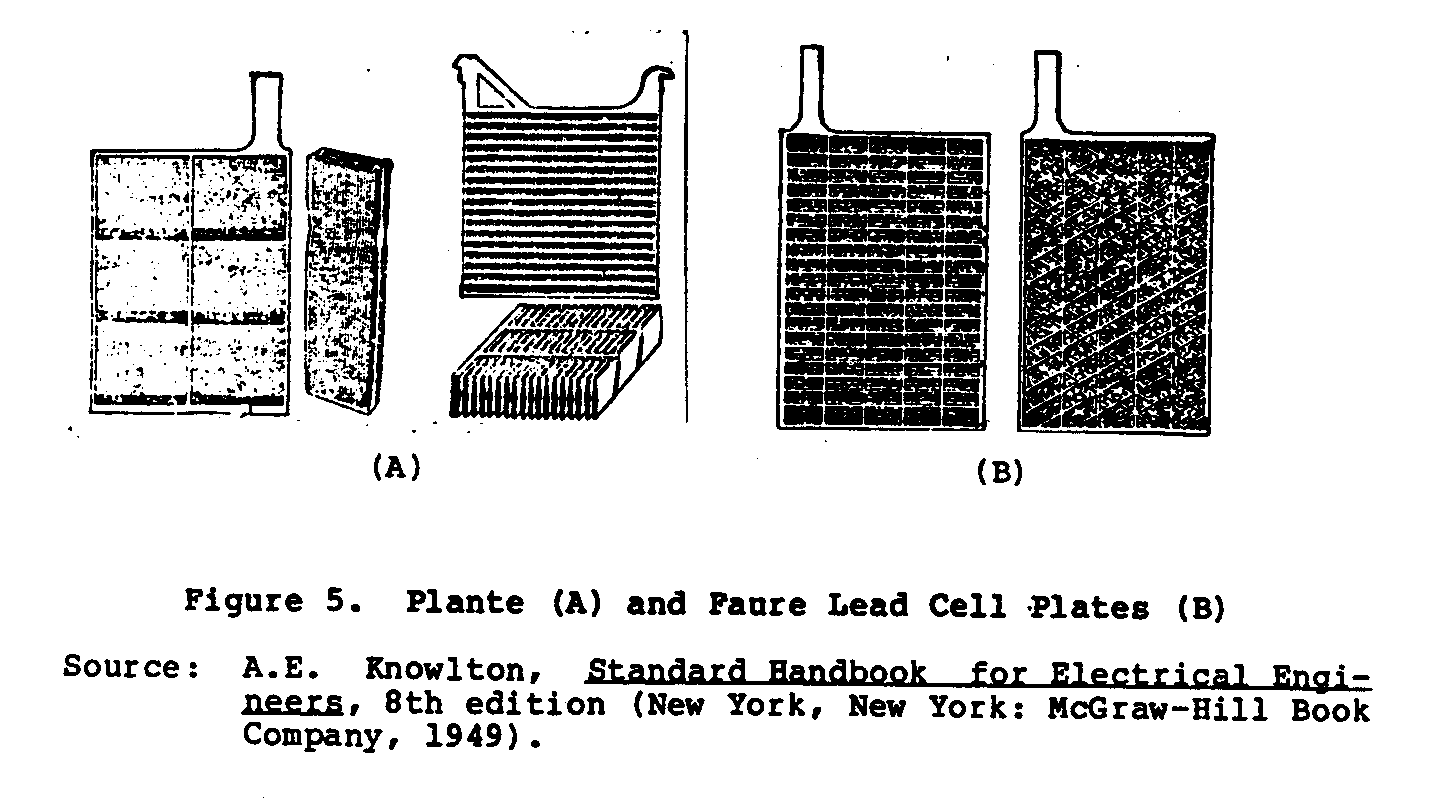
la Plante-tipo di costruzione che il materiale attivo è elettricamente formato di piombo puro da un processo di electrochemical dal piombo metallico della griglia che sostiene. Nella Faure-tipo il materiale attivo è applicato alla griglia che sostiene nella forma di un follwed della pasta da un setting, asciugando, e formando operazione.
Figuri 5 show il Plante (Un) e Faure (B) cella di piombo plates. Il riunioni di cella sono brasate insieme per formare positivo e negativo gruppi che sono interfogliati insieme per costituire il completi batteria che Separatori di cell. sono messi tra gli elettrodi, e l'elemento completo è messo in un contenitore e sealed. Il uso di piatti grandi con limiti di spaziatura vicini la resistenza interna della batteria ad un livello basso. Figure 6 show un scorciato

prospettiva della cella di deposito di piombo.
Durante scarico il materiale di batteria di ambo i piatti è convertito in piombo sulfate. L'ammontare di solfato di piombo formò piatti di onthe e l'ammontare di acido perse dall'elettrolito è in esatto proporzioni alla percentuale di scarico. Le prese di azione inverse luogo quando la cella è addebitata. Cella di che reazioni chimiche sono rappresentato dall'equazione seguente; comunque, questo è un forma semplificata come l'azione attuale molto è complicata più.
* Batteria ampere-ora tassando è basato su una 8-ora scarico normalmente percentuale.
Al piatto positivo:
PB[O.SUB.2] + HS[O.SUB.4][SUP. -] + [3H.SUP.+] + 2E.SUP. ------> PB[SO.SUB.4] + 2[H.SUB.2]O
Al piatto negativo:
Pb + HS[O.sub.4][sup. -]-----> Pb[SO.sub.4] + [H.sup.+] + [2e.sup. -]
La reazione di cella combinato per scarico e carica è espressa dall'equazione seguente: licenzia
------------->
Pb[O.sub.2] + Pb + 2[H.sub.2] S[O.sub.4] <= == == = 2Pb[SO.sub.4] + 2[H.sub.2]O + energia elettrica
solforico
acido di plate di plate i piatti di
<-------------;
addebita Su scarico l'acido separa dall'elettrolito e forme un combinazione chimica coi piatti, cambiandolo per condurre solfato.
Come continua scarico, acido supplementare è disegnato dal elettrolito fino a che corrente cesserà fluire. L'acqua, formò dalla perdita di acido ai piatti, abbassa il rimanendo specifico gravità * * dell'elettrolito. in comune pratica, scarico è sempre fermò prima i piatti hanno completamente sulfated, perché una volta completamente il sulfated, la condizione di batteria non può essere convertita indietro a materiale attivo su carica. Su carica l'azione inversa luogo di prese: l'acido nei piatti di sulfated è guidato posteriore in l'elettrolito, ed il S[O.sub.4] combina con idrogeno nell'acqua formare acido solforico e supplementare ([H.sub.2][SO.sub.4]).
Elettrolito per celle di piombo-acido è diluire acid. solforico Per un batteria pienamente addebitata alla quale la gravità specifica varia da 1.200 1.30 e quando licenziò 1.150 (acqua pura misura 1.00) . Il la gravità specifica è misurata da un idrometro di siringa-tipo come
mostrato in Figura 7, e valori sono temperatura corretta. * Il simbolo e - bancarelle per elettroni. * * La gravità specifica è definita come il rapporto di peso di un determinato volume di una sostanza ad un volume uguale di acqua pura. La tensione di una cella di piombo è approssimativamente 2.10 volt a nessun carico ma è più alto quando essendo addebitato. tensione Normale su carica è 2.15 volt e come la cella si avvicina a carica piena questo valore rapidamente gli aumenti a tra 2.5 e 2.6 volt. Questo più tardi l'intervallo di carica è noto come il " periodo " che gassa. Gassando del elettrolito ad alcuna durata durante addebitando dovrebbe essere evitato come il percentuale di carica è high. Come una cella anche arriva pienamente il suo finale condizione addebitata, un alto corrente non è consigliabile come questo eccesso corrente decompone l'acqua nell'elettrolito che è guidato via nella forma di benzina.
La batteria di piombo-acido ha molti svantaggi: (1) celle sono temperatura sensibile e perde il potere in temperature fredde; (2) piatti di cella tendono ad affibbiare e distorcere su sostenuto, alto corrente ripari, e (3) cura speciale si deve osservare quando una batteria è non usato per periodi lunghi, le celle vogliono altrimenti solfato.
Batterie di nichelio-ferro
Il nichelio-ferro o batteria alcalina furono sviluppate per superare il svantaggi inerenti della cella di piombo-piatto. è un radicale partenza da lui in costruzione ed operazione. Nel Stati Uniti che questa batteria è noto come la " cella di Edison, " chiamò dopo il suo inventore Tommaso A. Edison. Figure 8 show la costruzione

di un cell. tipico Il piatto positivo consiste di acciaio tubi che contengono idrato di nichelio e nichelio aggiunsero in alternato layers. dei quali Il piatto negativo è formato spianano scatole di acciaio o tasche che sono perforate ed impaccarono con granuli di ossido di ferro. Griglie di foglio-acciaio sostengono questi tubi e tasche che sono lanciato insieme formare cella positiva e negativa Cella di groups. terminali ed il contenitore di acciaio sono nichelio placcato. Tutti i separatori e parti isolanti sono fatte di gomma. La cella usa un elettrolito di 21 soluzione di percento di potassa caustico che contiene un piccola quantità di idrato di lithium.
La chimica di questa cella è complicata completamente, ed il chimico reazione che accade nella cella è completamente diversa da quello del piombo cell. che L'elettrolito si comporta come soltanto un conducendo mezzo e non entra in combinazione con alcuno del materiale di piatto attivo durante operazione. la Sua gravità specifica resti praticamente continuo sul ciclo completo di carica e discharge. Condition di carica di batteria o scarico è determinato da un voltmeter che legge e non dalla gravità specifica di l'electrolyte. che La reazione di cella di batteria alcalina è:
licenzia ------------------> [Fe.sub.2] + 2NiOOH + KOH + 2[H.sub.2]O-------> [Fe.sub.2][(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elettrico <------; <-----------------; l'energia di CHARGE
La tensione di ogni cella è approssimativamente 1.50 volt su apra circuito, ma è più alto su carica ed abbassa sotto le condizioni di carico. Queste batterie sono date ad un'ampere-ora capacità tassando basò sulla loro percentuale di scarico su alla finale tensione di 1.00 per cell. che delle stime correnti sono basate su una 5-1/2-ora continuo licenzi percentuale, mentre altri sono basati su una 3-1/2-ora percentuale.
Diversamente da batteria di piombo-cella, non è tensione minima sotto quale questo tipo di cella non può essere licenziato. infatti, questa cella può essere licenziato azzerare volt, cortocircuitato ai suoi terminali ed andato via in questa condizione per un periodo indefinito. Questo è il metodo dal quale una batteria alcalina è messa in deposito.
Questa cella può essere fatta pagare troppo accidentalmente anche, addebitò nel direzione sbagliata, e cortocircuitò momentaneamente senza danno. Batterie alcaline non sono ferite gelandosi ed un elettrolito con una gravità specifica di 1.200 a 15.5[degrees]C (60[degrees]F) gela solido a -66[degrees]C (-87[degrees]F). che L'elettrolito di questa cella gradualmente deteriora durante uso ed eventualmente deve essere cambiato.
I vantaggi principali della cella di nichelio-ferro sono: (1) è estremamente luce e dovendo forte alla sua costruzione di acciaio; (2) offre un indefinitamente la vita lunga; e (3) supera il problema di sulfating di cella della batteria di piombo-acido. Il capo svantaggio è suo alto prima costi e resistenza interna ed alta.
Batterie di nichelio-cadmio
Nichelio-cadmio o le batterie di Nicad, un relativamente somma nuova a celle di deposito, stato sviluppato in Europa. che Queste batterie consistono di riunioni interfogliate di piatti positivi e negativi montate in un contenitore di acciaio sigillato. Il materiale attivo e positivo, nichelio idrossido, ed il materiale attivo e negativo, ossido di cadmio è incassato in tasche di acciaio identiche, eccellentemente perforate. I piatti è fatto su di file di queste tasche che sono crespate e formato in acciaio frames. riunioni di piatto Positive e negative è lanciato insieme a sbarre di autobus di acciaio pesanti. Plate che gruppi sono interfogliato e separò da verghe di plastica e sottili. La cella elettrico terminali e caso sono nichelio placcato. L'elettrolito è un soluzione di potassa caustico e specialmente purificato (idrossido di potassio) dissolto in acqua distillata. Figure 9 show una vista scorciata
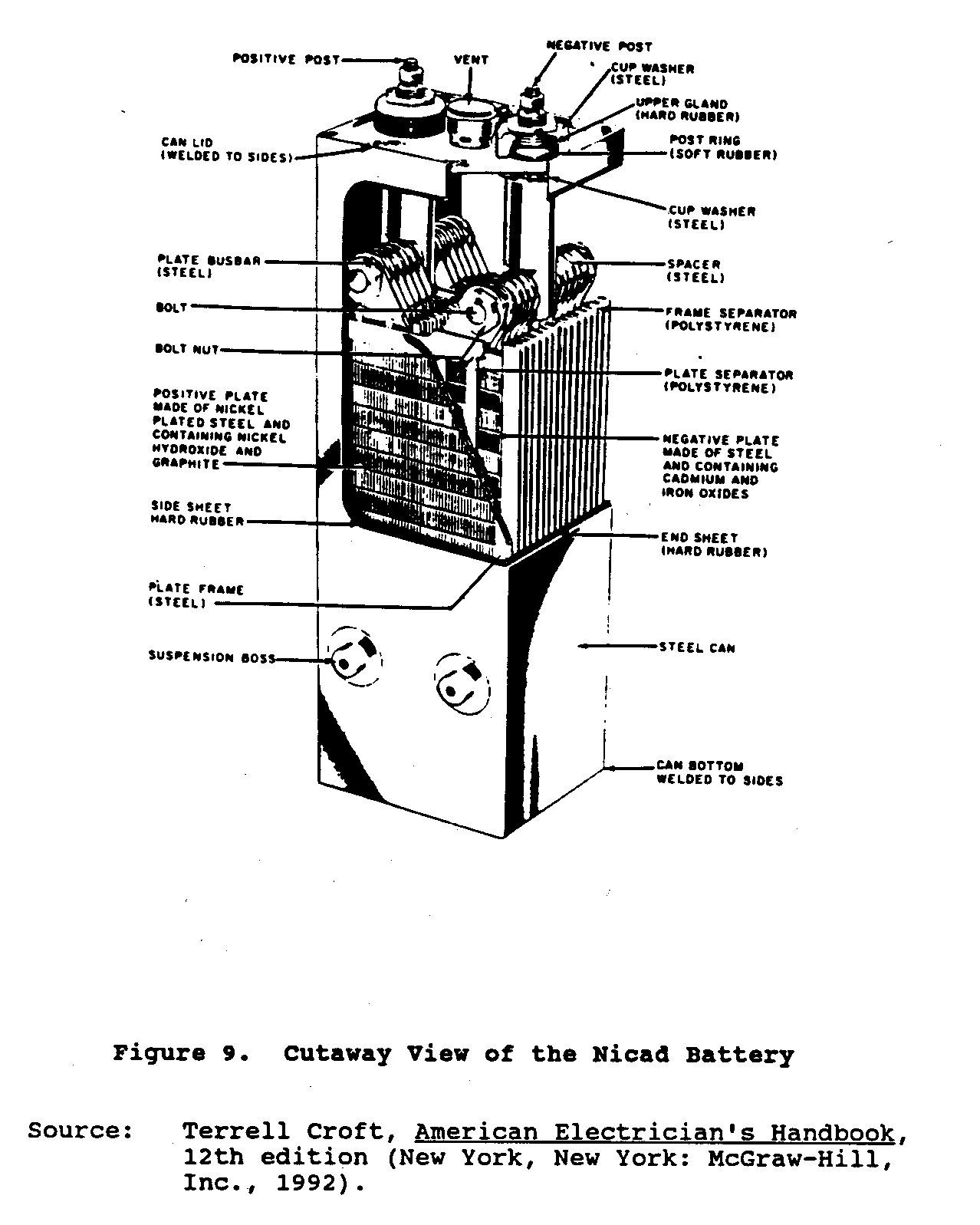
della batteria di Nicad.
La reazione di cella semplificata è:
addebita <-------------------; Cd + 2NIOOH + KOH + 2[H.sub.2]O------> Cd[(OH) .sub.2] + 2Ni[(OH) .sub.2] + KOH + elettrico <------l;'energia di --------------------> licenzia
Durante carica o licenzia della cella, c'è praticamente no cambi nella gravità specifica dell'elettrolito. Like il Cella di Edison, il risuoli funzione dell'elettrolito è agire come un bigliettaio per il trasferimento di ioni di idrogeno da un elettrodo a l'other. La tensione che tassa di ogni cella è 1.20 volt su apra circuito; quando collegato ad un carico esterno, questa tensione rimane, onestamente continuo su a verso 90 percento di suo tassò capacity. L'ampere-ora che tassa delle celle di Nicad è basata su un finale tensione di scarico di 1.10 volt per cella. Diversamente da Edison celle, le batterie di Nicad saranno danneggiate finito-licenziando ripetuto sotto la loro cella minima che tassa di 1.10 volt. le batterie di Nicad abbia una temperatura serie conduzione da -51[degrees]C (-60[degrees]F) a 93[degrees]C (200[degrees]F).
Le batterie di Nicad sono vibrazione e colpo resistente a causa di loro costruzione di acciaio; tenga bene la loro carica durante lungo inattivo periodi; mantenga una fonte di tensione continua durante scarico; e non è danneggiato da prezzo eccessivo. nel quale Queste batterie possono essere montate alcuna posizione su discharge. Come la cella di Edison, la batteria di Nicad ha un alto prima costi come comparato con la batteria di piombo-acido; comunque, questo costo alto è compensazione dalla loro vita più lunga span. Un paragone di piombo-acido, alcalino e le batterie di Nicad sono presentato in Tavola 2.
Table 2. Paragone di Piombo-acido, Nichelio-ferro e Batterie di Nichelio-cadmio
l'Operating Cella Vita Typical Temperatura l'Energia di la Carica di / Cell Serie la Densità di Discharge Costo TYPE VOLTAGE ([IL DEGREES]C) (WH (*) /KG) (CYCLES) ($/WH (*))
Piombo-Acid 2.0 20 a 30 37 1200-1500 .08 Nichelio-Iron 1.2 2.2 a 46 29 Nichelio-Cadmium 1.25 (-51) a 93 33
* Watt-ore
Procedure di Manutenzione generali per Batterie di Deposito
Manutenzione corretta è essenziale per servizio senza problemi e continuato di deposito batteries. Mentre la costruzione di cella è diversa per i molti tipi, manutenzione è simile per tutti i tipi e consiste delle procedure generali e seguenti:
1. Keep celle puliscono ed asciutto;
2. Check livello di elettrolito regolarmente;
3. Keep batterie sempre addebitarono; e
4. Keep le impurezze di qualche i generi fuori di celle come loro vogliono ha un effetto dannoso ed eventualmente la rovina them. Never usa alcuni attrezzi o utensili (idrometri, imbuti ecc.) che è usato per riparare elettroliti altri diversi da quello richiesto per quella batteria specifica, specialmente attrezzi usarono per batterie di piombo-acido.
5. Refer alle raccomandazioni di fabbricanti e tiene un nota di manutenzione scritto.
L'elettrolito della cella di piombo-acido non richiede mai sostituzione a parte perdita a causa di spargimenti fortuiti. However, nell'Edison e le celle di Nicad c'è un deterioramento graduale del loro elettrolito, quale eventualmente deve essere sostituito sulla vita del batteria.
BIBLIOGRAPHY/SUGGESTED READING L'ELENCO
BAUMEISTER, T., ED. Il Manuale di Standard di Mark per Ingegneri Meccanici. 7 Edizione. New York, New York: Libro di McGraw-collina Società di , 1967.
CARR, C.C. L'Elettricista americano di arte il Manuale. 8 Edizione. New York di , New York: Società del Libro della McGraw-collina, 1961.
Fink e Batey. Manuale Standard per Ingegneri Elettrici. 11 Edizione di . New York, New York: Società del Libro della McGraw-collina, 1978.
Hubert, Charles I. Preventative Manutenzione di Attrezzatura Elettrica. New York di , New York: Società del Libro della McGraw-collina, 1969.
Knowlton, A.E., Manuale Standard per Ingegneri Elettrici. 8 Edizione di . New York, New York: Società del Libro della McGraw-collina, 1949.
Enciclopedia di McGraw-collina di Scienza e la Tecnologia. 5 Edizione. New York di , New York: Società del Libro della McGraw-collina, 1982.
Timbro ed i Principi di Bush. dell'Ingegneria Elettrica. 3 Edizione. New York di , New York: Wiley e Figli, Inc., 1946.
Lupo, Stanley. Guide a Misurazione Elettronica e Laboratorio Practices. Rupi di Englewood, New Jersey: Sala di Prentice, Inc. di , 1977.